ギブズ

解離していないときの圧力P idealとすれば、 解離平衡時の圧力P obsを測定すれば解離度aは直ちに計算できる。 一方、などの応用領域においては、熱力学系で に寄与する有効エネルギーのみに意味があり、それを評価する量として が考案されている。 可逆反応なので、AからBへの反応もBからAへの反応も生じると言う事です。
20
解離していないときの圧力P idealとすれば、 解離平衡時の圧力P obsを測定すれば解離度aは直ちに計算できる。 一方、などの応用領域においては、熱力学系で に寄与する有効エネルギーのみに意味があり、それを評価する量として が考案されている。 可逆反応なので、AからBへの反応もBからAへの反応も生じると言う事です。
20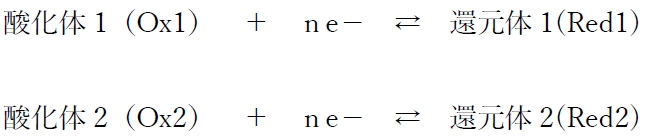
もちろんこの場合も水と水蒸気からなる部分系の体積は大きく変化する。 「科学は歴史をどう変えてきたか その力・証拠・情熱」p160-161 マイケル・モーズリー&ジョン・リンチ著 久芳清彦訳 東京書籍 2011年8月22日第1刷• 前節では、水の自由エネルギー変化は水蒸気に比べて大きくないので、その変化を無視して議論したのだが、ここではその効果を考慮して議論してみようということです。
18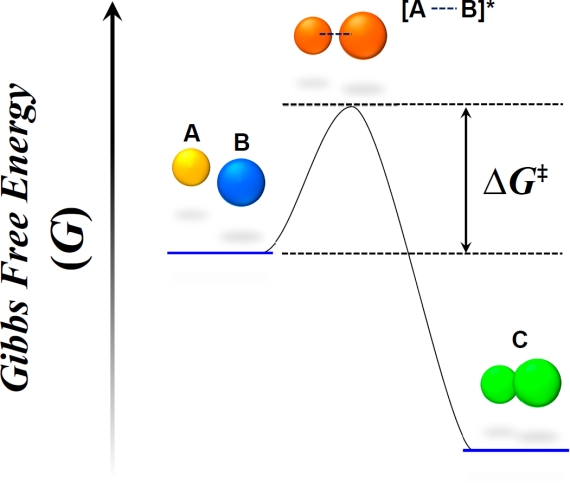

するとA状態のエネルギーは減少して、B状態のエネルギーレベルは上昇していきます。 この論争を 活力論争 と言う。 pdf )• それに対して、現実の物理化学的な問題を扱う際には、質量モル濃度(溶質の物質量を溶 媒の質量で割ったもの)やモル濃度(溶質の物質量を溶 液の体積で割ったもの)が便利である。
5さらにK P298の値が互いに逆数の関係に成っているのもその為です。 まず、生物代謝で身近な化合物の二酸化炭素 CO 2 の標準生成ギブズエネルギーを考えます。 化学反応における温度依存性を考える上で重要な式である。
5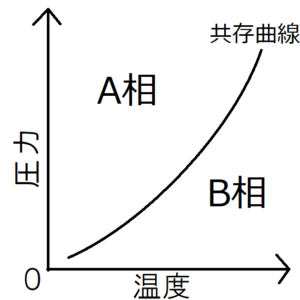

初めの状態でSO 2、O 2、N 2(不活性ガス)、SO 3がそれぞれ、a、b、c、0モル存在したとする。 化学変化の基礎(エンタルピー、エントロピー、ギブズエネルギー) このページでは、化学変化が自発的に起こる指標であるギブズエネルギーと、ギブズエネルギーを理解する上で大事なエンタルピー、エントロピーについて解説します。 『物理学辞典』 培風館、1998年。
18