国際新型コロナ細胞治療研究会。 <新型コロナに対する幹細胞治療による治験を実施中>新たにアメリカ合衆国及びメキシコでの薬事承認申請を実施 申請準備のための契約を本日締結|CENEGENICS JAPAN株式会社のプレスリリース
テラで緊急告知 「テラの株取引に反社会的勢力がマスコミを利用し株価操縦、調査で確証を得る」国際新型コロナウイルス細胞治療研究会


また、VBI社のワクチンに添加する免疫アジュバントとしてE6020の原薬を提供しました。 CENEGENICS JAPAN株式会社 先端医療支援事業を手掛けるCENEGENICS JAPAN 株式会社(本社:東京都中央区、以下「セネジェニックス・ジャパン」)は、幹細胞治療の研究開発を行うテラ株式会社(本社:東京都新宿区、代表取締役社長:平智之 以下「テラ」)と共同でプロジェクトにて、メキシコイダルゴ州に薬事申請しておりました「SARS-CoV-2 による急性呼吸窮迫症候群(ARDS)患者の治療目的の経静脈投与によるエクソソーム及びヒト間葉系幹細胞の使用の安全性と有効性に関する第二相比較試験」(以下、本試験)に関して、2020年9月2日(メキシコ時間)にメキシコイダルゴ州より薬事承認(以下、本承認)を取得しましたので、お知らせいたします。
2
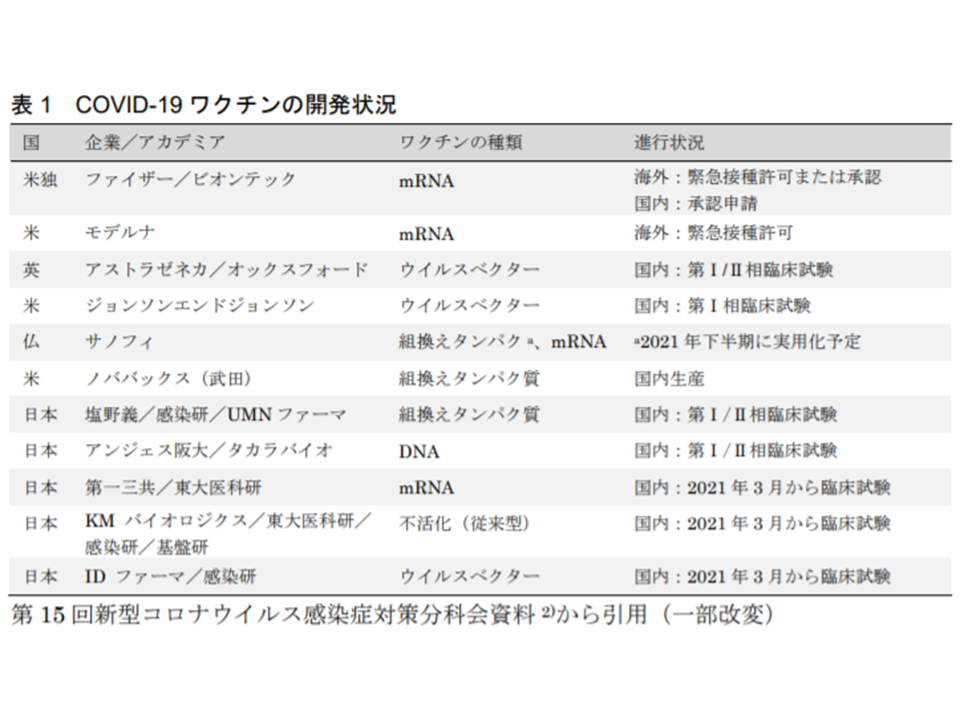
製薬協加盟各社による、治療薬・ワクチンの研究開発の取り組みについて|新型コロナウイルス感染症に対する製薬協の取り組みについて|日本製薬工業協会

COVID-19に対する抗体カクテル療法について、日本における開発権および独占的販売権を2020年12月にスイスのロシュ社より取得しました。 (以下「セネジェニックス・メキシコ」)は、既にMSCsの臨床応用を北米で展開しています。 本結果を受け、日本・コロンビアで同治療法の国際共同治験を検討します。
<幹細胞治療によって、”新型コロナウイルス撲滅” を目指すプロジェクト> 対コロナ新薬「プロメテウス」が、メキシコ・イダルゴ州にて薬事承認 日本国内でも国際共同治験を検討中

テラと当社は、今年の4月27日の治療薬共同開発研究の記者発表以来、一貫して、新型コロナウィルスの重症化の原因は、サイトカインストーム(免疫の暴走)であることを主張し続けて来ました。 PR 今後は、プロメテウス社が申請主体となり、速やかに連邦衛生リスク対策委員会(COFEPRIS)への薬事申請を進め、メキシコ連邦政府による薬事承認を取得するべく取り組んでまいります。 研究投資プロジェクト・プロメテウスと共に、COVID19の治療としてのこの細胞治療が全メキシコ国民に使用してもらえるように、連邦政府によるこの治療薬の薬事承認を求め、(プロメテウス・バイオテック株式会社の社長である)セルヒオ・アルバ氏と協力・協働していく所存でございます。
テラで緊急告知 「テラの株取引に反社会的勢力がマスコミを利用し株価操縦、調査で確証を得る」国際新型コロナウイルス細胞治療研究会

最新の情報は以下リンクよりご覧ください。
5
新型コロナ 治療薬の候補物質を発見 国立国際医療研究センター

2名は現在も人工呼吸器をつけた状態です。
4
<セネジェニックス研究所と幹細胞治療のテラによる共同事業> 新型コロナウイルスに対する日本初の“幹細胞”治療法開発に着手 メキシコにて計75名のコロナウイルス患者に対する臨床研究を本日より開始|CENEGENICS JAPAN株式会社のプレスリリース

そのため、患者への安定的かつ迅速な対応が期待できます。 MSCs は、自分の身体から取得するため、投与時の安全性が高く、倫理的問題が少ないと考えら れ、再生医療分野での応用が期待されている幹細胞です。 データおよび情報の共有: Data Sciences Instituteとのパートナーシップのもと、COVID-19に関するデータや情報を提携先と共有するための社外プラットフォームの開発を進めています。
<セネジェニックス研究所と幹細胞治療のテラによる共同事業> 新型コロナウイルスに対する日本初の“幹細胞”治療法開発に着手 メキシコにて計75名のコロナウイルス患者に対する臨床研究を本日より開始|CENEGENICS JAPAN株式会社のプレスリリース


ai1ec-fa-star-half-empty:before,. 上記の新薬について、テラ社は、日本で薬事承認を目指しており、この方針は維持されますが、アメリカ合衆国又はメキシコでの薬事承認が先行して得られた場合、特例承認されたレムデシビルのように薬事承認が容易になる可能性があります。 【今後のスケジュール】 5月13日 メキシコにて、臨床研究を開始 5月27日 臨床研究の中間報告 7月中 メキシコでの臨床研究終了、結果報告 変更となる可能性もございますが、今秋中の国内治験開始、新薬承認を目指しております。 AMEDが実施する、「新型コロナウイルス感染症 COVID-19 に対する治療薬開発」において、当社を代表機関とする研究開発プロジェクト「新型コロナウイルス感染症 COVID-19 の重症化を阻止する治療薬の開発」が採択され、4つの分担研究機関(株式会社 カン研究所、国立研究開発法人国立国際医療研究センター、国立大学法人長崎大学、公立大学法人横浜市立大学)とともに、TLR4拮抗剤エリトランおよび抗FKN フラクタルカイン 抗体E6011を用いたCOVID-19治療薬の開発をめざす共同研究を開始しました。
16
<幹細胞治療のテラとセネジェニックス研究所による共同事業> 国内初、新型コロナウィルス感染症に対する幹細胞治療 臨床試験を開始|PRTIMES|時事メディカル|時事通信の医療ニュースサイト

微生物病研究所、BIKEN財団、医薬健栄研が有するワクチン開発・実用化にむけた研究資源・ノウハウを活用し、すみやかな臨床試験開始を目指します。
13
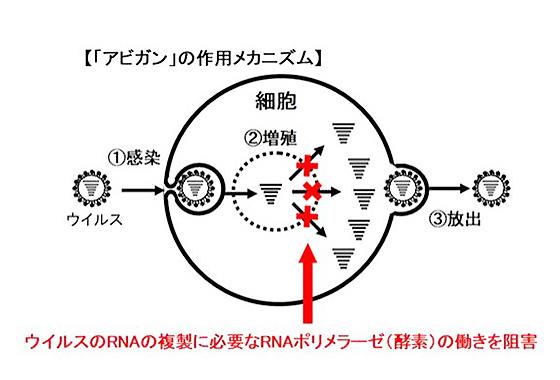
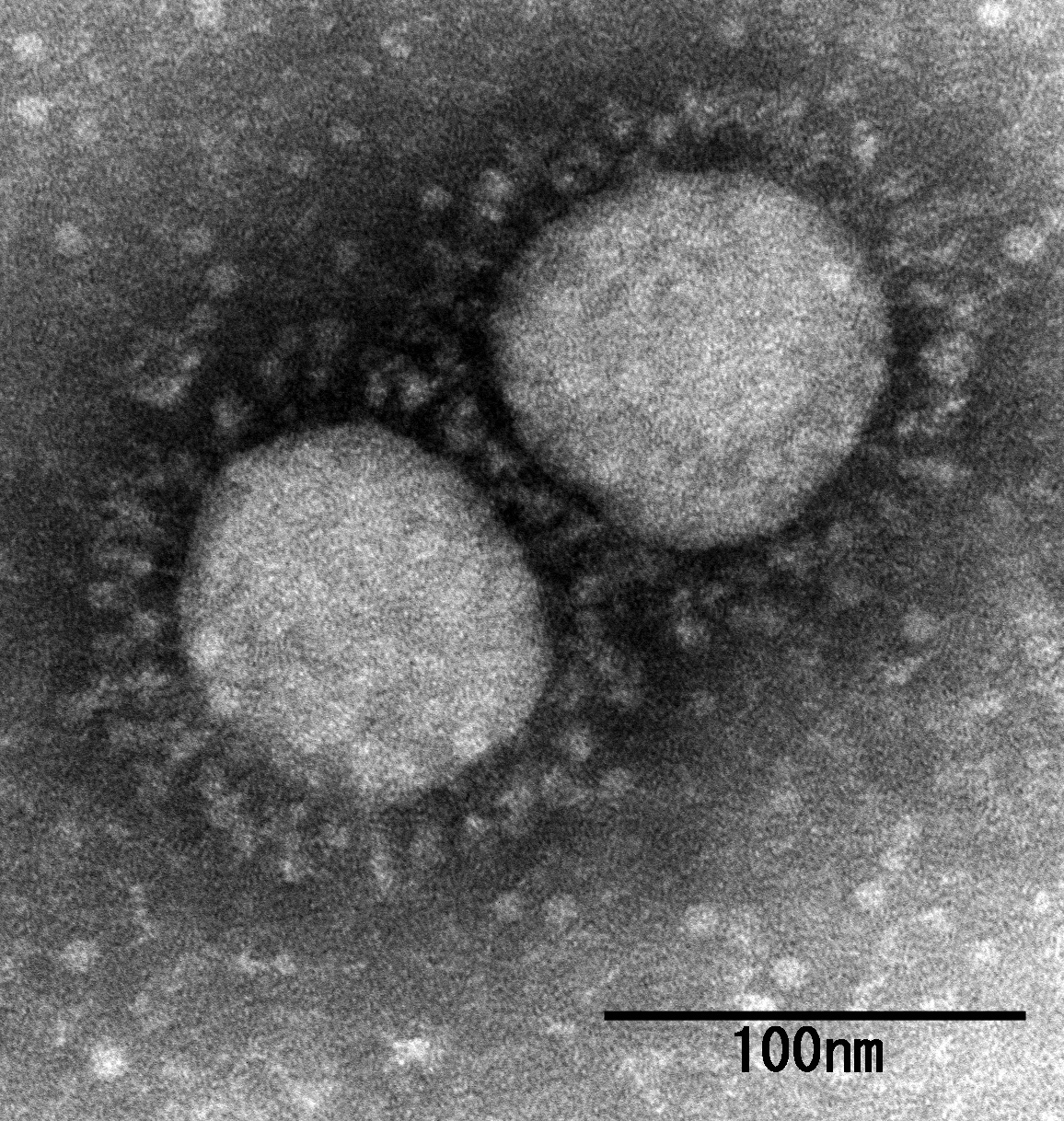
新型コロナウイルスの仕組みと幹細胞による治療

(以下「セネジェニックス・メキシコ」)が保有し、メキシコ国内で承認を得ている米国FDAの基準を満たした臍帯由来幹細胞(UC-MSC)を用いて、コロナウィルス感染症により中等度以上の呼吸器症状が出現している新型コロナ肺炎患者(18歳~75歳)総計75名を対象に、臨床研究を行っております。 特例承認を受けるには、以下のようないくつかの条件がある。
1
















