電離平衡


つまり、酸の水溶液を薄めると、平衡は右に移動して、電離度は大きくなっていくのです。 急性毒性• これは滴定によって酢酸ナトリウムが生じ,未反応の酢酸と共に緩衝溶液となっているためである。 塩酸と酢酸の場合を例に、電離度を見てみます。


つまり、酸の水溶液を薄めると、平衡は右に移動して、電離度は大きくなっていくのです。 急性毒性• これは滴定によって酢酸ナトリウムが生じ,未反応の酢酸と共に緩衝溶液となっているためである。 塩酸と酢酸の場合を例に、電離度を見てみます。
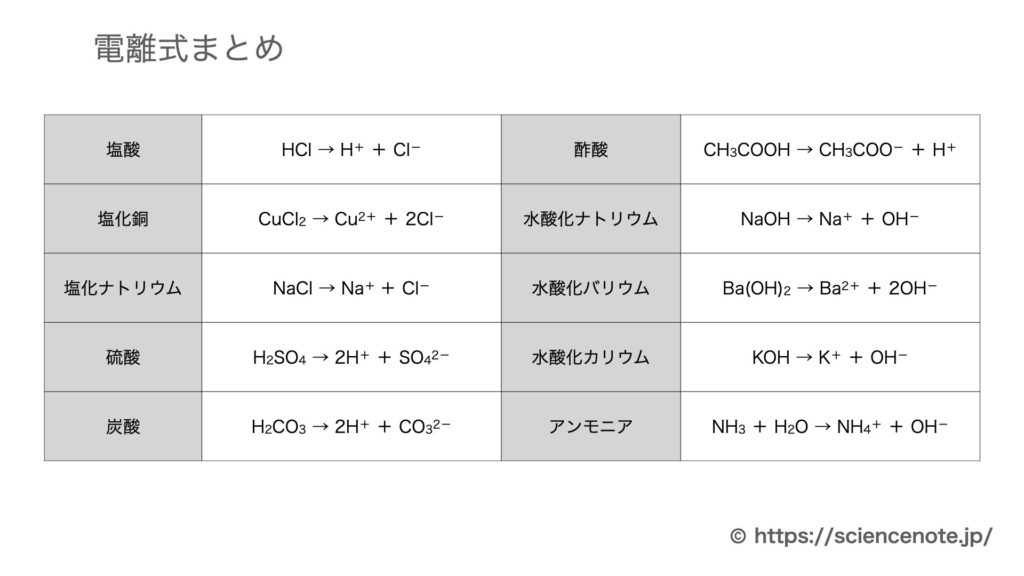

ウィルキンソン著, 中原 勝儼訳 『コットン・ウィルキンソン無機化学』 培風館、1987年、原書:F. 公式を丸暗記するというよりかは、公式の導入が入試で問われやすいです。
18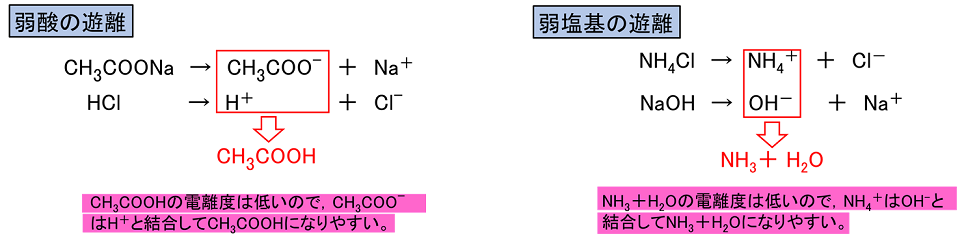
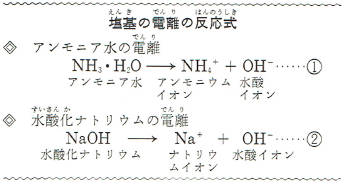
アンモニアの場合出発物質を水溶液中でもNH3としています。 塩基の強弱は、同じ濃度の場合、水に溶かしたときに電離して生じる水酸化物イオンの数で決まります。


NH4OHは現在どの教科書でも使われていません。 酸を加えて染料液を中和すると、赤い色素が水に溶けにくくなって、繊維との親和性が高まり染着しやすくなります。 デンマークのブレンステッドとイギリスのローリーは,1923年にそれぞれ独自にプロトンの授受で定義しています。
10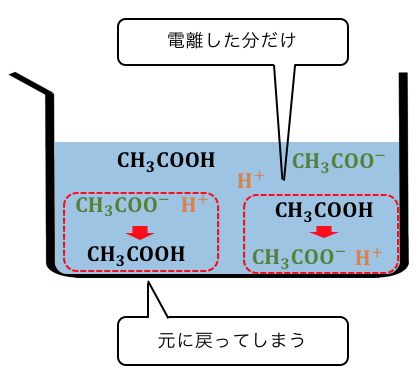
。

ここで、平衡状態にある酸 HA の水溶液を 2 倍に薄めたと仮定しましょう。 酢酸 CH 3COOHのような弱酸が水に溶けると,一部が電離して,酢酸イオン CH 3COO -と水素イオン H +が生成して,平衡状態になる。 1.酸性の性質には,どのようなものがありますか? 酸味がある,青色リトマス紙を赤色に変える,緑色のBTB溶液を黄色に変えるなど 2.アルカリ性の性質には,どのようなものがありますか? 赤色リトマス紙を青色に変える,緑色のBTB溶液を青色に変える,無色のフェノールフタレイン溶液を赤色に変えるなど 酸性を示す物質が酸であり,英語でacidといいます。
8